Строение атома
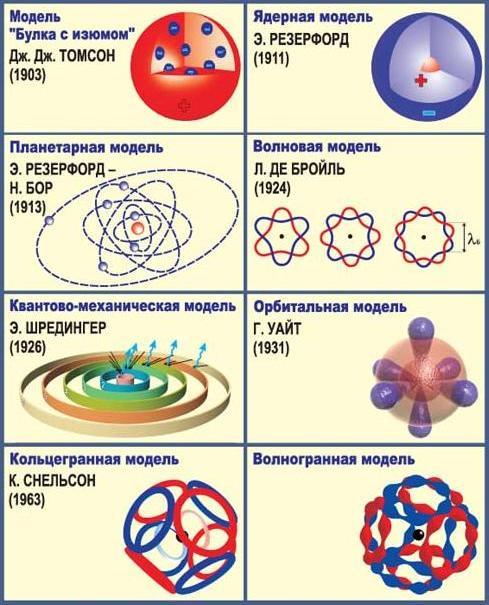 История открытия строения атома была долгой и запутанной. Предлагались разные модели строения атома.
История открытия строения атома была долгой и запутанной. Предлагались разные модели строения атома.
Английский ученый Эрнест Резерфорд в 1911 г. предложил схему строения атома, получившую название ядерной (планетарной) модели атома.
Согласно этой модели, атом состоит из положительно заряженного ядра и движущихся вокруг него электронов. Почти вся масса атома (более 99,96 %) сосредоточена в его ядре, диаметр которого приблизительно в 100 000 раз меньше диаметра всего атома.
Если изобразить размеры ядра атома водорода точкой всего в 1 мм, то границы атома должны были бы находиться на расстоянии 50 м.

Ядро атома состоит из частиц:
протонов p (положительно заряженные частицы) и
нейтронов n (электронейтральные частицы).
| Частица | Символ | Относительная масса | Относительный заряд |
| Протон | p | 1,007 ≈ 1 u | 1+ |
| Нейтрон | n | 1,009 ≈ 1 u | 0 |
| Электрон | e– | 1u : 1840 | 1- |
Физический смысл атомного номера: атомный (порядковый) номер элемента в периодической системе равен относительному заряду ядра его атомов.
Атомный Заряд Число Число
номер = ядра = протонов = электронов
элемента атома в ядре в атоме
Например, атомный номер лития Li равен 3. Следовательно, относительный заряд ядра его атома равен 3+ (т. е. содержит три протона), а вокруг ядра вращается три электрона.
На основании всего сказанного, современная формулировка периодического закона звучит так:
