Периодическая система химических элементов: периоды и группы
Опираясь на периодический закон, Д. И. Менделеев построил естественную классификацию химических элементов периодическую систему химических элементов. Ее графическим изображением является таблица, которая так и называется — периодическая система химических элементов. Формы таблицы различны (их известно более 700). В настоящее время используется следующая:

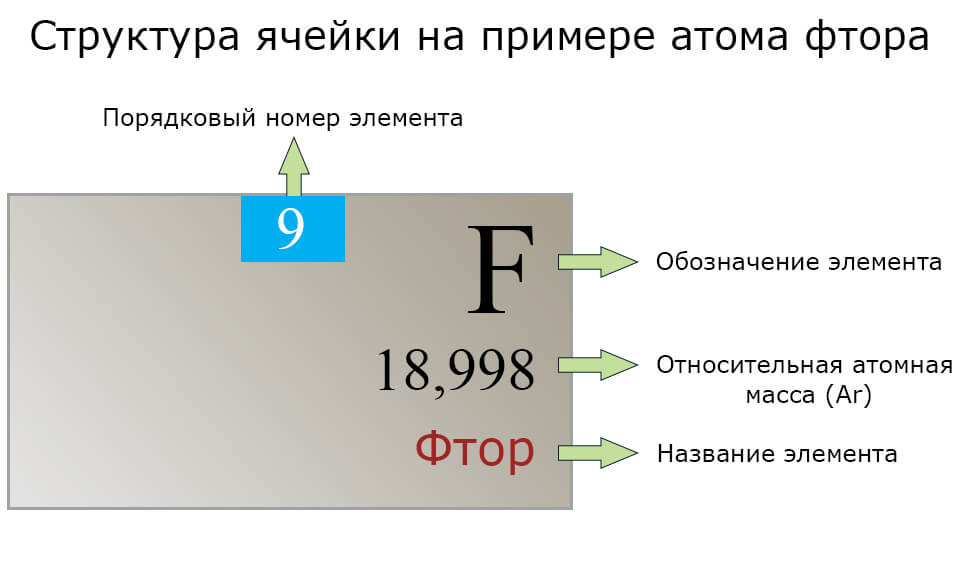
Каждый химический элемент имеет свою ячейку, где указан его химический знак, порядковый (атомный) номер, относительная атомная масса.
Горизонтальные ряды элементов называются периодами, а вертикальные столбцы — группами. Это основные структурные единицы периодической системы. Следовательно, каждый химический элемент имеет свой атомный номер, находится в определенном периоде и определенной группе.
Всего в таблице семь периодов. Их номера указаны цифрами, стоящими слева. Каждый период содержит определенное число химических элементов:
1-й период — 2 элемента
2-й период — 8 элементов Малые периоды 1 – 3
3-й период — 8 элементов
4-й период — 18 элементов
5-й период — 18 элементов Большие периоды 4 – 7
6-й период — 32 элемента
7-й период — 32 элемента
В периодах наблюдается постепенное ослабление металлических и усиление неметаллических свойств атомов и простых веществ элементов, только переход идет от щелочного металла к благородному газу через большее число элементов, более плавно.
Всего в таблице восемнадцать групп, пронумерованных арабскими цифрами. Кроме того, группы имеют традиционную нумерацию римскими цифрами, сохранившуюся со времен Д. И. Менделеева: от I до VIII с добавлением латинских букв А или В.
Группы А часто называют главными. Они включают все элементы первых трех (малых) периодов, а также нижестоящие элементы больших периодов. В этих группах находятся как металлы, так и неметаллы. Граница между этими двумя типами элементов обычно выделяется жирной ломаной линией. Эта граница достаточно условна, так как некоторые элементы, находящиеся возле нее, могут проявлять как металлические, так и неметаллические свойства. Некоторые главные группы имеют свои собственные названия. Так, например, IА-группа — это группа щелочных металлов + водород Н, IIА-группа — группа щелочноземельных металлов + бериллий Ве и магний Mg, VIIА-группа — группа галогенов, VIIIА-группа — группа благородных газов и т. д.
Между I—IIA- и III—VIIIA-группами располагаются переходные элементы групп В. Группы В иногда называют побочными. В них находятся только элементы больших периодов, они все являются металлами. Все группы имеют собственные названия, обычно связанные с названием первого элемента в группе. В каждой группе находятся элементы со сходными химическими свойствами их простых веществ. Римские цифры номера группы указывают, как правило, высшую, т. е. максимальную, валентность элементов в соединениях с кислородом.
Атомы некоторых элементов проявляют и другие значения высшей валентности (Cu, Au) или просто не имеют кислородных соединений (Не, Ne, Аr).
