Ионная связь. Понятие об ионах
Особенности ионной связи:
1.различие ЭО между атомами велико, поэтому общая электронная пара практически полностью смещается в сторону более электроотрицательного атома.
2.связь между атомами типичных металлов и типичных неметаллов.
Рассмотрим в качестве примера образование молекулы NaCl.
| Na | Cl | |
| количество электронов на внешнем слое | 1 е– | 7 е– |
| сколько не хватает электронов до завершения внешнего слоя | 7 е– | 1 е– |
| что проще сделать, чтобы завершить энергетический слой | отдать 1 е– | взять 1 е– |
| в ходе перехода электрона получили | 8 е- на внешнем слое | 8 е- на внешнем слое |
| образовался ион | Na+ | Cl– |
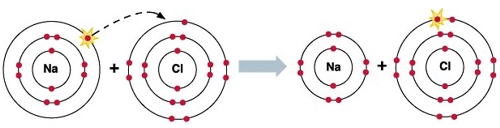

Ионная связь возникает за счет электростатического притяжения разноименных ионов.
Ионы – устойчивые заряженные частицы, которые образуются в результате приема или отдачи электронов атомами.
Положительно заряженные ионы называют катионами.
Отрицательно заряженные ионы – анионы.
C помощью ионной связи образуются и такие соединения, в которых имеются сложные ионы (OH−, NO3– , NH4+ и др.), например NaOH или KNO3.
