Химические свойства оснований
Основные свойства оснований зависят от положения элемента в периодической системе:
1.слева направо по периоду основные свойства гидроксидов ослабевают;
2.в группах А сверху вниз происходит усиление основных свойств;
3.в случае, когда металл образует несколько оснований (гидроксидов), основные свойства более выражены у того из них, в составе которого степень окисления атома металла меньше, например, Mn(OH)2 – гидроксид с более слабыми основными свойствами, чем Mn(OH)4.
Химические свойства нерастворимых оснований
| Нерастворимое основание + | Продукты реакции | Химическое уравнение реакции | Дополнение |
| не изменяют окраску индикаторов | |||
| диссоциируют | Сu(OH)2 ⇔ CuOH+ + OH–
CuOH+ ⇔ Cu2+ + OH– |
Диссоциируют обратимо, ступенчато в незначительной степени | |
| разлагаются
(тип разложение) |
основный оксид + вода | Сu(OH)2 = CuO + H2O
Mg(OH)2 = MgO + H2O |
Легко разлагаются при нагревании |
| кислота
(тип обмен) |
основания + кислота | Cu(OH)2 + H2SO4 = CuSO4 + 2H2O
Mg(OH)2 + 2HNO3 = Mg(NO3)2 + 2H2O |
Реакция нейтрализация |
| кислотные оксиды
(тип обмен) |
соль + вода | 3Mg(OH)2 + P2O5 = Mg3(PO4)2 + 3H2O
Cu(OH)2 + SO3 = CuSO4 + H2O |
Только жидкие и твердые кислотные оксиды участвуют в реакции |
Химические свойства щелочей
| Растворимые основания + | Продукты реакции | Химическое уравнение реакции | Дополнения |
| Изменяют окраску индикаторов | 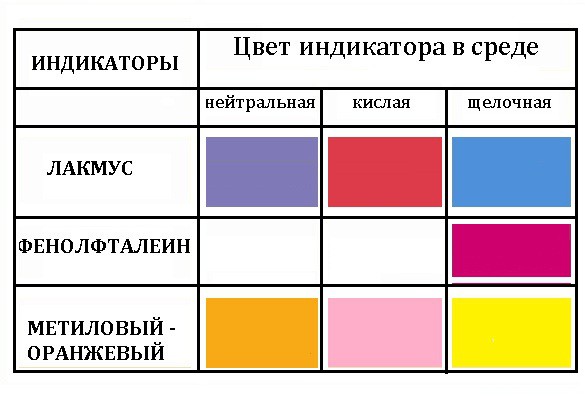 |
||
| диссоциируют | KOH ⇔ K+ + OH–
NaOH ⇔ Na+ + OH– |
В водных растворах щелочей находится избыток гидроксид ионов, поэтому среда щелочная. Диссоциируют полностью | |
| кислотный оксид
(тип обмен) |
соль + вода | 2KOH + SO2 = K2SO3
3Ba(OH)2 + P2O5 = Ba3(PO4)2↓ + 3H2O |
|
| амфотерный оксид
(тип обмен) |
соль + вода | 2KOHтв + Al2O3 = 2KAlO2 + H2O↑
2NaOHтв + ZnO = Na2ZnO2 + H2O↑ |
При сплавлении с твердой щелочью при температуре |
| комплексная соль | 6KOHр-р + Al2O3 + 3H2O = 2K3⌈Al(OH)6⌉
2NaOHр-р + ZnO + H2O = Na2⌈Zn(OH)4⌉ |
Участвуют водные растворы щелочей | |
| кислота
(тип обмен) |
соль + вода | 2NaOH + H2S = Na2S + H2O
3KOH + H3PO4 = k3PO4 + 3H2O |
Реакция нейтрализация |
| амфотерный гидроксид | соль + вода | 2NaOHтв + Zn(OH)2 = Na2ZnO2 + 2H2O↑
3KOHтв + Al(OH)3 = KAlO2 + 2H2O↑ |
Щелочь в твердом состоянии, процесс сплавление при температуре |
| комплексная соль | 2NaOHр-р + Zn(OH)2 = Na2⌈Zn(OH)4⌉
3KOHр-р +Al(OH)3 = K3⌈Al(OH)6⌉ |
Щелочь в водном растворе | |
| соль | соль + основание | 2KOH + MgCl2 = Mg(OH)2↓ + 2KCl
NaOH + NH4NO3 = NaNO3 + NH3 + H2O |
1.Исходная соль должна быть растворима в воде
2.Должен образоваться газ, осадок или слабый электролит |
| с некоторыми неметаллами (галогенами, Si, S, P) | соль + вода (водород) | 2KOH + Cl2 = KCl + KClO + H2O
6KOH + 3Cl2 = 5KClO3 + KCl + 3H2O (t) 2NaOH + Si + H2O = Na2SiO3 + 2H2↑ 6KOH + 3S = 2K2S + K2SO3 + 3H2O |
|
| c амфотерными металлами | комплексная соль + водород | 2Al + 6KOH +6H2O = 2K3⌈Al(OH)6⌉ + 3H2↑
Zn + 2NaOH + 2H2O = Na2⌈Zn(OH)4⌉ + H2↑ |
Щелочь в растворенном состоянии |
| разлагаются при нагревании | основный оксид + вода | 2LiOH = Li2O + H2O
Ca(OH)2 = CaO + H2O |
плавятся и кипят без разложения NaOH, KOH, CsOH, RbOH; LiOH плавится (4300С) без разложения, при кипении разлагается (≈9500С) |
Химические свойства амфотерных гидроксидов
| Амфотерные основания + | Продукты реакции | Химическое уравнение реакции | Дополнения |
| не изменяют окраску индикаторов | |||
| диссоциируют | Al(OH)3 ⇔ Al(OH)+ + OH–
Al(OH)+ ⇔ AlOH2+ + OH– AlOH2+ ⇔ Al3+ + OH– |
диссоциируют обратимо в незначительной степени | |
| щелочь | соль + вода | 2NaOHтв + Zn(OH)2 = Na2ZnO2 + 2H2O↑
3KOHтв + Al(OH)3 = KAlO2 + 2H2O↑ |
Щелочь в твердом состоянии, процесс сплавление при температуре |
| комплексная соль | 2NaOHр-р + Zn(OH)2 = Na2⌈Zn(OH)4⌉
3KOHр-р +Al(OH)3 = K3⌈Al(OH)6⌉ |
Щелочь в водном растворе | |
| кислота | соль + вода | Al(OH)3 + 3HNO3 = Al(NO3)3 + 3H2O | |
| основный оксид | соль + вода | Al(OH)3 + K2O = KAlO2 + 3H2O↑
Zn(OH)2 + BaO = BaZnO2 + H2O↑ |
при нагревании
амфотерный гидроксид проявляет кислотные свойства |
| кислотный оксид | соль + вода | 2Al(OH)3 + 3SO3 = Al2(SO4)3 + 3H2O↑
3Zn(OH)2 + P2O5 = Zn3(PO4)2 + 3H2O |
при нагревании
амфотерный гидроксид проявляет основные свойства |
| карбонаты | соль+ углекислый газ + вода | 2Al(OH)3 + CaCO3 = Ca(AlO2)2 + CO2↑ + 3H2O | при сплавлении с твердыми карбонатами |
| разлагаются при нагревании | амфотерный оксид + вода | 2Al(OH)3 = Al2O3 + 3H2O | |
Задание 1. В отличие от воды разбавленный водный раствор гидроксида калия растворяет:
а) Na
б) Be
в) MgO
г) Al
1) а, б, г
2) б, г
3) б, в, г
4) а
Задание 2. Укажите ряд, в котором оба гидроксида можно получить растворением соответствующего металла в воде:
1) Fe(OH)2, Zn(OH)2;
2) Be(OH)2, Pb(OH)2;
3) Mn(OH)2, Ca(ОН)2;
4) Sr(OH)2, Ba(OH)2.
Задание 3. Порошок гидроксида алюминия обработали небольшим количеством гидроксида калия. Раствор осторожно упарили, сухой остаток осушили и взвесили, затем прокалили. Масса остатка уменьшилась на 30%. Найдите массовые доли веществ в нем.
